在创新药等生物制药的过程中,建立菌种库的意义在于利用菌种库系统进行充分的质量检测并以此最大程度的控制和减少污染和菌种的性质改变。科研人员为了达到菌种库建立的目的,在建立菌种库时需要菌种库具备足够数量的菌种和维持菌种的均质性,用以确保研发和生产过程中所用的菌种的来源的一致性。
关键词
三级种子库
菌种库的构建
什么是三级菌种库?
菌种建库建立的三级种子库包括
1. 原始种子库(pre-master cell bank/research cell bank, PCB/RCB)
2. 主代种子库(master cell bank,MCB):从原始种子批传代、扩增后保存的为主种子库
3. 工作种子库(working cell bank,WCB):从主种子库进行批传代、扩增后保存即为工作种子库
每批种子库都应按规程的要求进行保管、检定和使用。为了保障生物制品的安全性,必须对其进行严格的检测,确定其达到相关技术标准要求。
三级菌种库不仅仅是简单的将菌种按照传代或者特性分为三个级别,而是对于菌种的保存与运用设置了三种基础的质量和程序要求,以确保菌种在长期的、大规模的生产应用中的稳定性和可溯源性等。
主菌种库与工作菌种库的区别
主菌种库是从PCB分离出来的单菌落,然后对该单菌落经过传代,增殖后混成均质菌悬液,定量分装于冻存管,并采取适当方法保存的用于制备工作菌种库的菌种来源。
工作菌种库是由主菌种库再传代增殖后,混成均质菌悬液,定量分装于冻存管,并采取适当方法保存的用于商业化生产的菌种来源。发酵所用的菌种除了常规的检测指标,如菌落形态外观、生产能力和其他生化指标外,还需要检测:如污染菌检査(微生物、真菌、支原体的检测分析)、组分检测、孢子量检测等才能被作为工作菌种库保存和使用。
在实际运用过程中,部分企业将主菌种库和工作菌种库简单的以传代次数和保存条件进行划分。
这种区分方法是绝对错误的,在短期生产或无后续研究的情况下或许不会出现缺漏,但只要进入长期、大规模生产阶段,这种区分方法就带来工作菌种的质量和性质不稳定等诸多问题。出现以上问题的主要原因是没有理解主菌种库与工作菌种库之间的关系。
1、来源的不同,MCB来源于初始菌株的单菌落,如诱变后的高产菌种,在经过稳定性验证后,从这一高产单菌落中进行增殖获得的一系列的菌悬液。WCB是从MCB扩增而来,但并不出自于MCB的单菌落。
2、对法规理解偏差,如果每年的使用量特别小,当MCB足以支持生产需要时,便没有必要设置WCB。
3、MCB和WCB在工艺和质量放行的标准上存在不同。一般MCB比WCB在使用和标准上更严格。
什么样的菌种才可以作为工作菌种?
微生物发酵产品通常会采用化学、物理诱变方法或者基因技术对微生物菌种进行选育或基因改造,得到一个更高产能效率的新菌种。得到的高产菌株,如果经过生产能力,传代稳定性,组分检测、孢子量等检测指标,尤其是杂质指纹比较后,确定没有问题后就可以建立新的主菌种库,而用于商业化生产。
菌种库的构建
菌种库构建过程主要需要注意以下几个方面
1. 建库用菌种的溯源性
2. 菌种建库过程合规性
3. 建库菌种的检定要求
4. 菌种传代稳定性研究
一、溯源性
为保证菌种的可溯源性菌种库构建资料要求具备基因、载体和宿主细胞的来源及改造过程。其来源明确清晰,切实可靠,其演化历史也必须清楚。
目的基因:
为确保目的基因的可溯源性菌种库必须确定其来源、设计和改造过程,并且要求来源明确清晰,历史演化过程清楚。
表达载体:
为保证表达载体的可溯源性菌种库构建资料要求具备表达载体的来源、名称、结构等信息,说明重组质粒的构建和检定过程。载体来源应当清楚,明确其出处以及可靠性。
宿主细胞:
宿主细胞的来源要明确,提供其名称、生物学特性,检定结果等信息。
二、菌种建库过程合规性
建库流程:依照法规规定,从筛选到的高表达菌株单克隆经反复纯化扩增验证后,冻存于-80℃,即为原始种子库。取一只原始种子,复苏后扩增验证,然后混合一定浓度的甘油后在-80℃冻存,即为主种子库。取主种子进行复苏后扩增验证,然后混合一定浓度的甘油后在-80℃冻存,即为工作种子库。所有的种子都要严格记好株名、批号、编号、冻存日期、分装数量、放置位置及取用记录等。
①需在GMP体系完成建库工作,建库流程、储存、运输过程都要形成SOP管理文件。
②保证均质性,如果是使用了多个容器培养,分装前需要有合适的方法充分混匀。
③为保证工作种子库、主种子库与原始种子库的生物学特性一致,建库过程中不得有单克隆挑选和菌种筛选的行为。
星耀小TIP:
GMP标准(药品生产质量管理规范)是为保证药品在规定的质量下持续生产的体系。它是为把药品生产过程中的不合格的危险降低到最小而订立的。GMP包含方方面面的要求,从厂房到地面、设备、人员和培训、卫生、空气和水的纯化、生产和文件。
三、建库菌种的检定要求
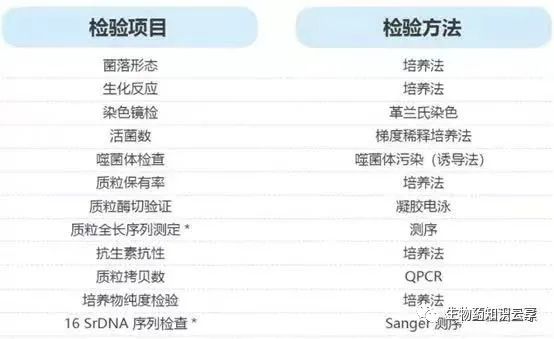
①菌落形态及抗生素抗性,考察菌种在含与不含抗生素培养基上生长的菌落形态及抗生素抗性。
②生化反应,考察工程菌是否具有典型的大肠杆菌生化反应。
③染色镜检,考察工程菌菌体形态及革兰氏类别。
④重组表达载体酶切检定,通过琼脂糖凝胶电泳鉴定重组质粒酶切后DNA片段大小符合理论值。
⑤基因序列测序,验证重组表达载体上的目的基因序列的正确性。
⑥电镜观察,通过电镜观察菌体形态,支原体、病毒样颗粒及其他微生物污染情况。
⑦菌体目的蛋白表达检定,通过SDS-PAGE检测分析重组质粒是否表达目的蛋白。
⑧菌体表达蛋白免疫原性检查,通过Western-blot检测分析重组质粒表达的重组蛋白是否具有正确的免疫原性。
《中国药典》三部中规定了细胞基质的质量要求,包括:细胞鉴别(种属、株及专属特性);外源因子污染检查(包括病毒性及非病毒性内外源因子);成瘤性及致瘤性检测;染色体核型;均一性及稳定性等。
四、菌种传代稳定性研究
根据《中华人民共和国药典》相关要求,种子库要开展传代稳定性研究,明确限传代次数,使用寿命,评估是否能够满足未来商业化生产需求。在开展传代稳定性研究时应在模拟实际的生产条件下开展。通常对重组质粒稳定性和表达稳定性研究的方法为:对种子库菌种多代次培养,通过双酶切检测与菌体PCR检测,确定传代50次后质粒是否丢失。通过对传代50代的菌液诱导培养后,对菌体表达的目的蛋白量进行SDS-PAGE检测,确定传代后的表达稳定性。
总结
综上所述,三级菌种库的建立不仅仅是为了为菌种的保存和追溯提供切实的依据,而且是在GMP审查以及IND申报时所必需的数据来源。因此在建立三级菌种库之时所需要考虑的不仅包括菌种库本身的基本要求,而且要把IND申报的要求考虑在内。在保证符合国家关于菌种库建立的要求之外,符合IND申报和GMP体系的要求。






