2020年,突如其来的新冠疫情席卷全球。新冠病毒传播速度快,感染面积大,毒株易变异等特点,导致疫情防控难度升级。为建立疫情防护屏障,人们需要在短时间内研发生产相应疫苗,并且快速、大规模生产和接种。
传统疫苗受制于研发周期长、成本高、生产难度大等原因无法快速高效地应对新冠快速传播和病毒变异迅速的特点。如,灭活疫苗或减毒疫苗从临床到上市研发周期长达10年,花费高达5-7亿美元。另外,传统疫苗涉及病原体,因此对疫苗的安全性、生产难度提出了较高要求。
面对全球性的疫情,如何快速、高性价比的控制病毒传播成为人类共识。消失在人们视野中多年的mRNA疫苗,因其苗研发周期短、生产相对简单,在这场疫苗竞赛中,崭露头角,重新获得了科学家、产业界人士的关注,并且对mRNA技术的最大化利用,造福人类健康,有了更加明确的方向和落地场景。
1.1 mRNA的定义
mRNA (信使核糖核酸) 通过“翻译”指导蛋白质的生产,是由DNA模板转录而来,携带遗传信息,指导细胞生产胞内蛋白、膜蛋白及胞外蛋白。
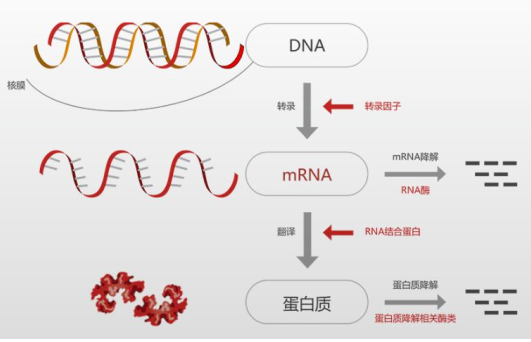
图1:mRNA转录翻译过程
1.2 mRNA的发展历程
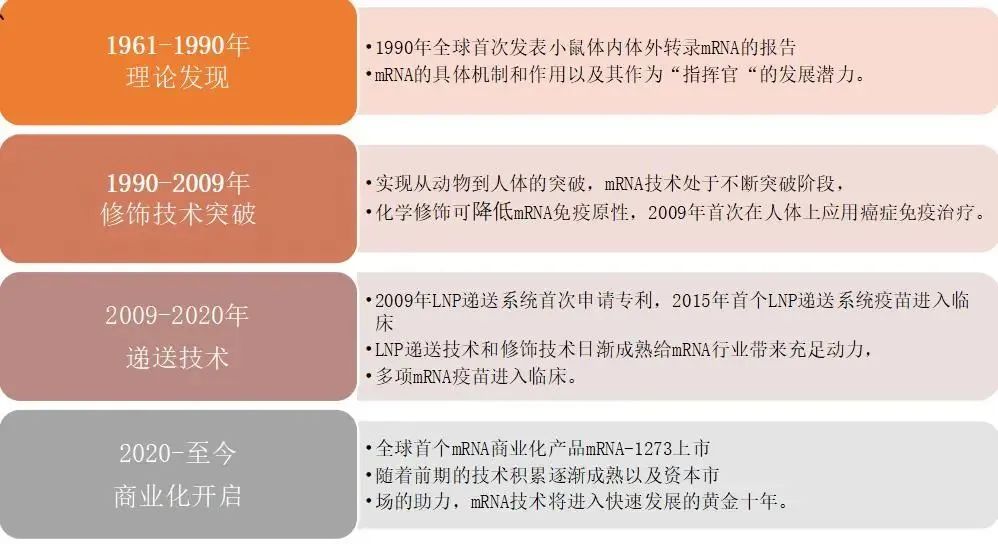
图2:mRNA发展历程
1.3 mRNA应用领域
mRNA因其技术优势,理论上能够表达任何蛋白质,可以防治多种疾病,因此mRNA可以作为一种极具潜力的通用技术平台。目前mRNA可应用于传染病预防、肿瘤免疫治疗、蛋白替代、CAR-T/M等,总体可分为三大类:预防疫苗、治疗疫苗、治疗药物,其中预防疫苗领域的布局最丰富,其次是治疗药物领域。
Nature Reviews Drug Discovery在2021年发文分析了全球31家mRNA公司,有77%的公司至少拥有至少一款mRNA预防性疫苗的公司达77%,拥有至少一款mRNA治疗性疫苗的公司达35%,拥有至少一款mRNA治疗性药物的公司达55%。
在76款预防性疫苗中,22%是用于预防COVID-19感染,77%用于预防其他感染性疾病;在32款治疗性疫苗中,21%与癌症相关;在72款mRNA治疗性药物,肿瘤药占13%,罕见病药物占20%,呼吸疾病药物占17%。
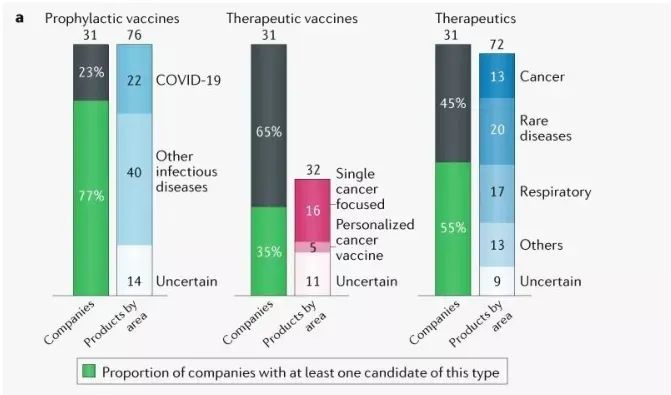
图3:mRNA应用分布比例
从产品开发进度上看,已有mRNA预防性疫苗产品获批上市或获得紧急使用授权(EUA),分别来自辉瑞/BioNtech和Moderna。mRNA治疗性疫苗和治疗性药物目前尚无获批的产品。总体而言,mRNA产品大多处于I期和临床前开发阶段。
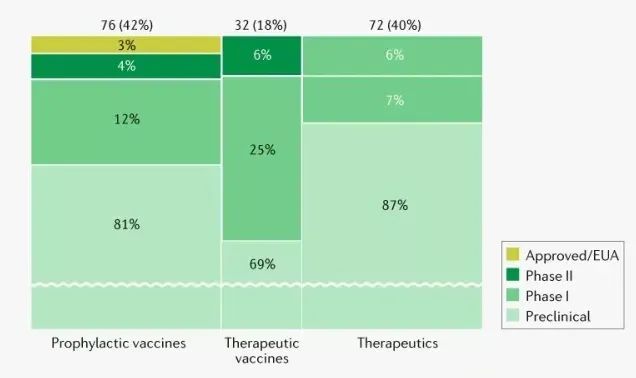
图4:mRNA应用进展
1.4 mRNA技术壁垒
以mRNA疫苗为例,生产过程中主要涉及到分子结构设计、递送系统的优化、生产工艺放大等诸多环节,每个环节都有关键技术壁垒或者工艺难点需要解决,如递送系统的专利问题、分子结构的优化等。
合适递送系统:mRNA分子较脆弱,基于这一特点,mRNA药物需借助递送系统进人体内从而发挥作用。因此找到合适的递送系统便成为最关键的部分,也是一家企业的技术实力和壁垒体现。
翻译效率提高并工艺放大:mRNA翻译效率的高低,是企业分子序列优化能力的直接体现。经过企业摸索具体工艺参数能够将实验室中试工艺放大并稳定生产,形成稳定的生产工艺,这也是企业核心竞争力的表现和技术壁垒。
1.4.1 mRNA递送系统简要介绍
1) 递送原因
由于mRNA较大(104–106Da)且带负电和可降解性,导致裸露的mRNA不容易穿过细胞膜的阴离子脂质双层并有效地渗入细胞质,因此如何将mRNA递送至细胞质中并及时指导蛋白质生产将成为核心。mRNA指导细胞生产所需的蛋白质,理论上可将编码相应蛋白质的mRNA通过一定手段运送到细胞质内,从而对所有蛋白质层面疾病发挥疗效。
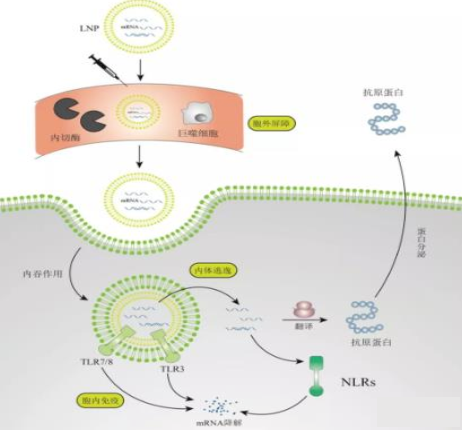
图5:mRNA递送路径
2) 递送难点
一个高效和优质的递送系统需要解决3个难点,分别是胞外屏障、内体逃逸、胞内免疫。
3) 递送系统
mRNA的递送系统以脂质纳米颗粒(LNP)为主,如国际上Moderna、BioNTech、CureVac以及国内除斯微生物的多数mRNA公司的递送系统均使用LNP。LNP为mRNA递送提供了许多好处,包括制剂简单、模块化、生物相容性和较大的mRNA有效载荷容量。LNP通常包括四种成分,可电离脂质/可离子化脂质、胆固醇、辅助磷脂/中性脂质、PEG修饰脂质,它们共同封装和保护脆弱的mRNA。不同分子及构成比例是各家LNP系统的主要差异所在:
可电离脂质/可离子化脂质:与mRNA在酸性缓冲液中形成纳米颗粒,使脂质带正电荷并吸引RNA;具有pH敏感性,与带负电的mRNA结合,可高效包载核酸药物,同时在酸性环境下被质子化,有助于内涵体逃逸;截至目前可用于RNA输送的可电离脂质包括:DODAP、DODMA、DLin-MC3-DMA(已用于siRNA药物patisiran)、C12-200、503O13、306Oi10、OF-02、TT3、5A2-SC8、SM-102(已用于抗SARS-CoV-2的Moderna疫苗mRNA-1273)、ALC-0315(已用于辉瑞疫苗BNT162b2)、含有多环金刚烷尾的脂质11-A-M58、含有环咪唑头的脂质93-O17S59等等。 中性脂质/辅助磷脂:稳定粒子,破坏内涵体稳定性,提高核酸递送效率; 胆固醇:是一种天然存在的脂质,通过填充脂质之间的空隙来稳定LNP结构,调节膜流动性,提高粒子稳定性,并有助于在摄取到细胞的过程中与内涵体膜融合。 PEG修饰脂质:提高粒子稳定性,减少粒子在体内与血浆蛋白的结合,延长体循环时间;
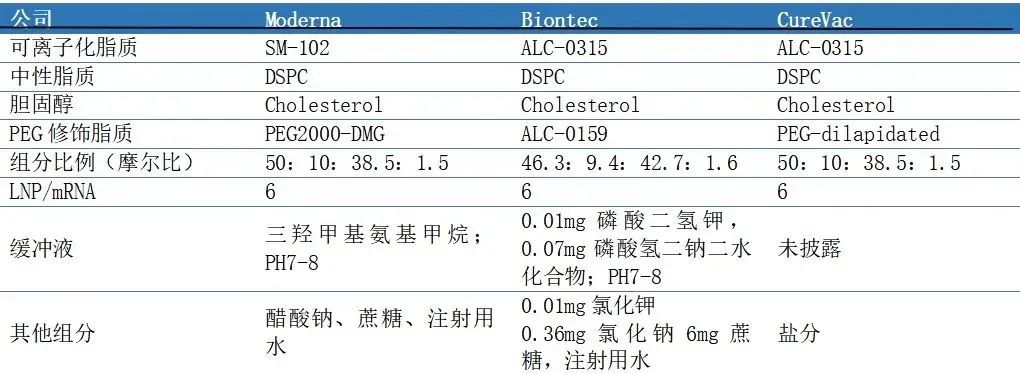
表1:Moderna、BioNTech和CureVac LNP构成
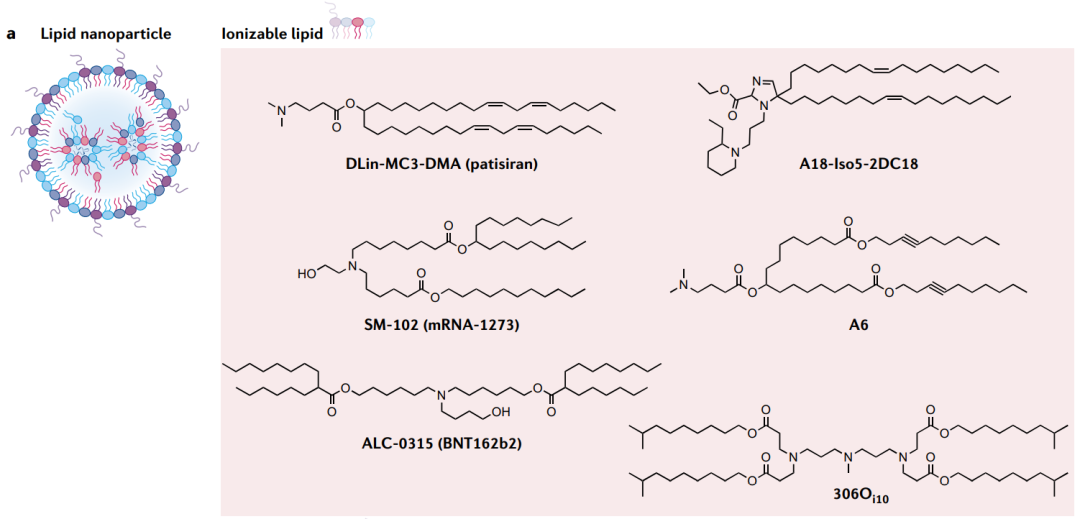
图6:LNP递送系统
聚合物和聚合物纳米颗粒临床进展不如LNP,但聚合物具有与脂质相似的优势,能够有效传递mRNA。阳离子聚合物将核酸浓缩成具有不同形状和大小的复合物,可通过内吞作用进入细胞。
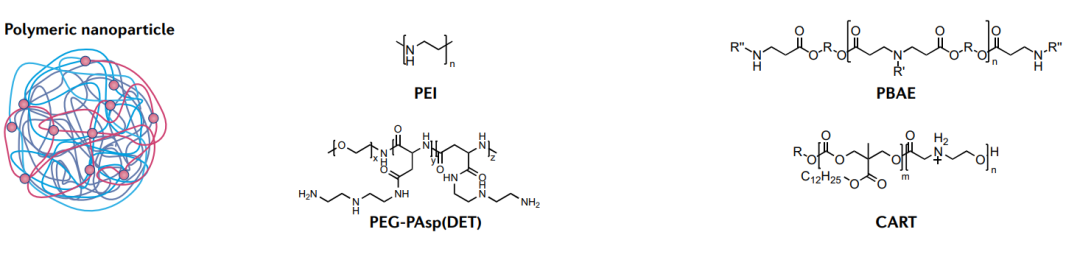
图7:聚合物和聚合物纳米颗粒递送系统
聚乙烯亚胺是研究最广泛的核酸传递聚合物。尽管其功效卓越,但由于其高电荷密度,其毒性限制了应用。此外,已经开发出几种毒性较小的可生物降解聚合物。例如,聚(β-氨基酯)在mRNA传递方面表现出色,尤其是对肺。
新型含脂聚合物电荷改变可释放转运体(CARTs)能有效地靶向T细胞,操纵T细胞是非常困难的,因此,CART是一种极具吸引力的传递材料,在mRNA疫苗和基因治疗领域具有巨大潜力。
多肽也可以将mRNA传递到细胞中,这要归功于其主链和侧链中的阳离子或两亲胺基(例如精氨酸),这些阳离子或两亲胺基与mRNA静电结合并形成纳米复合物。例如,含有重复的精氨酸-丙氨酸-亮氨酸-丙氨酸(RALA)基序的膜融合细胞穿透肽。富含精氨酸的鱼精蛋白肽在中性pH下带正电荷,也可以浓缩mRNA并促进其传递。鱼精蛋白与mRNA复合物激活识别单链mRNA的Toll样受体(TLR7,TLR8)通路,因此,它还可以作为疫苗或免疫治疗应用的佐剂。CureVac AG正在评估一种含有鱼精蛋白的递送平台RNActive,用于黑色素瘤、前列腺癌和非小细胞肺癌的临床试验。
角鲨烯阳离子纳米乳液也可以传递mRNA,这些纳米乳剂由油性角鲨烯核组成。一些角鲨烯制剂,如诺华的MF59,在FDA批准的流感疫苗中用作佐剂。MF59使注射部位的细胞分泌趋化因子,从而招募抗原呈递细胞,诱导单核细胞分化为树突状细胞,并增强抗原呈递细胞对抗原的摄取。角鲨烯基阳离子纳米乳剂从内涵体逃逸并将mRNA输送到细胞质中的机制尚不清楚。
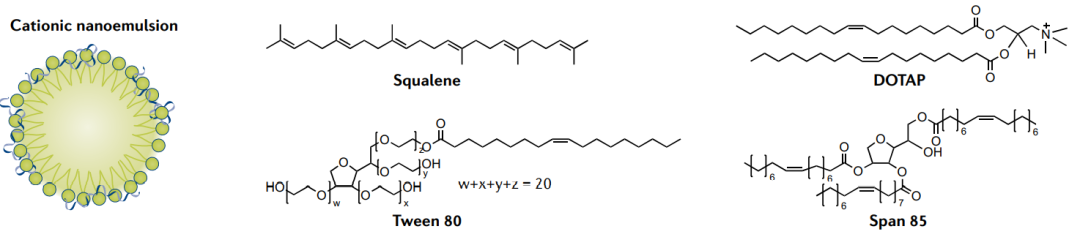
图8:其他递送系统
4) 专利突破并形成稳定的工艺参数
专利壁垒:目前Arbutus具有LNP递送系统的专利所有权(US8058069B2),其专利范围包含核酸、阳离子脂质、非阳离子脂质、缀合脂质以及各成分的比例,预计2029年到期。 工艺参数:即使递送系统的成分及配方已经公开但工艺参数依然是商业秘密。意味着即使企业知道如何使用合适比例的原材料进行LNP系统的配制,依然会面临着工艺参数稳定性的问题。 工艺参数未知的具体问题:LNP粒径是否均一、杂质是否有残留、阳离子脂质导致的细胞毒性、LNP的靶向性以及如何可控地释放包封药物等。
1.4.2 mRNA的序列优化
正确选择病毒的抗原序列:mRNA疫苗研发的关键,是找到最佳蛋白质抗原。由于不同的蛋白质是由不同的RNA序列编码。因此在选择特定病毒的正确抗原时必须非常谨慎,要保证疫苗包含RNA所编码的蛋白既安全又有效。
mRNA序列的优化:斯微生物通过与全球公司合作并借助“AI+云计算”技术,开发独特算法技术(proprietary),以实验数据矫正数字模型,并改善预测和序列设计的准确性和效率。与传统的序列优化平台相比,该技术可以把mRNA的表达效率提高3-4倍,并降低mRNA的降解比例。而Moderna等巨头公司,是与Amazon等合作解决序列优化的问题。
化学修饰可调节mRNA稳定性、翻译效率及免疫原性:mRNA的结构组成含有几个必要的元件,依次包括帽子结构(Cap)、5’UTR区、编码抗原蛋白的开放阅读框(ORF)、3’UTR区和Poly(A)尾结构。

图9:影响mRNA稳定性和表达效率因素
mRNA具有不稳定、免疫原性过高和翻译效率低等缺点,为提高mRNA的稳定性和翻译效率,必须对mRNA的元件进行设计。目前的策略是在mRNA分子中掺入化学修饰过的核苷酸,可显著提高其翻译效率,延长其半衰期,同时达到降低其免疫原性的目的。
Cap结构:Cap结构与mRNA的稳定性和免疫原性密切相关,还会影响mRNA的翻译效率。主要功能有:1)作为翻译起始的必要结构,为核糖体对mRNA的识别提供了信号;2)增加mRNA的稳定性,保护mRNA免遭5’→3’核酸外切酶的降解;3)作为自身识别信号,避免激活Rig-I及IFIT而导致的免疫抑制。通过引入抗-反转帽子类似物(ARCA),可以提高mRNA的翻译效率;此外,在ARCA基础上修饰Cap结构,还可以提高mRNA的稳定性。
5’UTR区:mRNA翻译效率的主要因素之一,是5’UTR区的结构特征。在真核细胞中,翻译开始前mRNA需要招募核糖体亚基结合到其5ʹm7Gcap上,但起始密码子又常常在5ʹm7Gcap下游较远的地方,所以核糖体亚基需要经过5ʹUTR到达起始密码子AUG处,从而开始翻译。因此,5ʹUTR的长度和结构对翻译的起始具有重要影响。此外,紧密的二级结构会阻止核糖体的结合,所以在设计mRNA时,5ʹUTR不能太长或太紧密。在设计mRNA时,应该避免在5ʹUTR区域引入上游开放阅读框序列和起始密码子AUG。上游开放阅读框序列是存在5ʹUTR的一段包含起始密码子和终止密码子的连续碱基序列,它可能会抑制ORF区基因的表达,也可能导致mRNA的降解,因此对蛋白表达具有负面影响。最后,在5ʹUTR区域引入强的Kozak序列可以加强起始密码子的识别,让mRNA更容易被翻译,避免错误启动。
开放阅读框(ORF):在mRNA的开放阅读框(ORF)中,将常用的密码子去替换不常用的密码子,即密码子优化,这一过程可以提高mRNA的稳定性和翻译效率。在开放阅读框(ORF)中,每相邻的3个核苷酸组成密码子,在翻译时代表某一种氨基酸。密码子的组成对mRNA的翻译效率和稳定性都有显著影响。同义密码子是指序列不同但是对应相同氨基酸的密码子,而不同生物常用的密码子组成都不相同。密码子优化是因为,将mRNA注射到人体内,原宿主的mRNA包含的密码子虽然对应相同的氨基酸,但是并不常用,导致mRNA进入人体后不稳定并且翻译效率低。此外,通过增加嘌呤和胞嘧啶(GC)含量也有一定正面效果。
3’UTR区:3’UTR区是mRNA不稳定因素的集中区域,其中AU富集序列(AREs)、AUUUA重复序列和GU富集序列(GREs)是3'UTR引起mRNA不稳定的最常见因素。因此,在合成的mRNA中应避免这些序列。3ʹUTR内的AU富集序列(AREs)是激活mRNA快速衰变的顺式作用序列,AREs上的AUUUA重复序列数量和位臵对Poly(A)尾的缩短和RNA降解有关键的影响。而该区域上的另一GU富集序列(GREs),在哺乳动物细胞中能与CELF1蛋白结合从而加快mRNA的衰变。此外,通过引入稳定元件,可以显著提高mRNA的稳定性,延长其半衰期。例如,BioNTech公司专利中使用了2个β球蛋白(β-globin)串联的3'UTR,这大大地增强了mRNA的稳定性。此外,人类α和β球蛋白的3'UTR可增强mRNA的稳定性和翻译效率,头尾排列的人类2个β-球蛋白的3'UTR可增加mRNA的稳定性。
Poly(A)尾:mRNA翻译效率和稳定性很大程度上受Poly(A)尾的影响。在翻译效率方面,Poly(A)尾和5ʹ帽的协同作用可以增加翻译效率;在稳定性方面,Poly(A)尾的去除是大多数真核mRNA降解的第一步和限速步骤,且Poly(A)尾的存在可以抑制mRNA的降解和脱帽。Poly(A)尾的重要作用决定了实验中对mRNA进行加尾处理的必要性。在体外为mRNA加尾有两种方式:第一种是先进行体外转录,再通过酶促多聚腺苷酸化将Poly(A)尾加到mRNA上;第二种是将Poly(A)尾序列加在模板上,直接通过体外转录合成带Poly(A)尾的mRNA。通过酶促反应进行加尾时,需要注意Poly(A)尾后若有其他碱基可能会影响其功效,因此应避免在体系中混入其他核苷酸。与此同时,最好将Poly(A)尾的长度保持在最佳的100至120个核苷酸。例如,在BioNTech公司公开的专利中,长度为120个核苷酸的Poly(A)尾有最高的稳定性和翻译效率。但由于酶促反应进行加尾受到温度、酶质量等反应条件的影响较大,导致Poly(A)尾长度无法保证完全一致,故在大多临床试验中只能保证加尾长度最少为多少,如果需要保证精准的Poly(A)尾长度则需采用第二种方法。
核苷酸类似物:通过使用核苷酸类似物可以提高mRNA的稳定性、降低免疫原性并且增加翻译效率。如:假尿苷(Ψ)、5-甲基胞苷(m5C)、N6-甲基腺苷(m6A)、5-甲基尿苷(m5U)和2-硫尿苷(s2U)等,其中尿嘧啶类似物在核苷酸修饰中较为常见。
疫苗原理:大部分的疫苗是通过递送抗原,使人体自发形成特异性免疫反应。免疫记忆形成后,若人体遭受病原体袭击,获得性免疫迅速反应,在病原体大规模感染其他细胞前,将病原体和易感染细胞消灭。
mRNA疫苗:mRNA疫苗是一种核酸疫苗,通过将病毒的部分mRNA片段注入人体细胞内产生抗原,再由此激发特异性免疫反应,形成免疫记忆效果。
mRNA疫苗治疗原理:mRNA治疗疫苗的原理是将编码抗原的mRNA通过不同的递送方式递送到人体细胞内,在细胞内翻译后产生相应的抗原蛋白,从而有效激起细胞免疫和体液免疫。
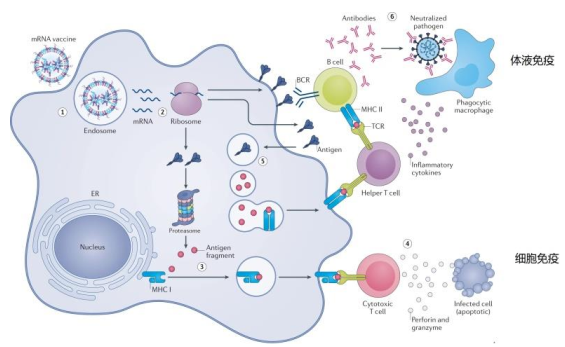
图10:mRNA治疗原理
03mRNA疫苗优势
传统疫苗的是体外生产,依赖于生物反应装置或鸡蛋中使用哺乳动物细胞。不同与传统疫苗的生产方式,mRNA疫苗只需在接种者体内经过一次转化就可以发挥作用。人体被mRNA疫苗作为“生物反应装置”。
研发周期短。研发成本相对较低。mRNA疫苗研发周期在一年左右,研发成本可控制在2亿美元以内。传统疫苗基本需要8年以上研发周期,耗费2-10亿美元的研发成本,DNA疫苗研发周期有所缩短,但一般也需4-7年。
安全性高。mRNA疫苗进入体内会经历自然降解过程,副作用能得到更精确控制,不存在整合、诱导基因突变和外源性病毒感染风险;
水溶性较好,更容易成药;
设计性强。可呈递多种抗原,可靶向递送至DC细胞;
可快速制备。通常传统疫苗的生产至少需要6个月时间,而mRNA疫苗由于高产量的体外转录反应和快速制剂的特点,在实现标准化生产的情况下30天内就可产成,疫苗的时效性在应对突发疫情尤其是病毒变异时分外重要。
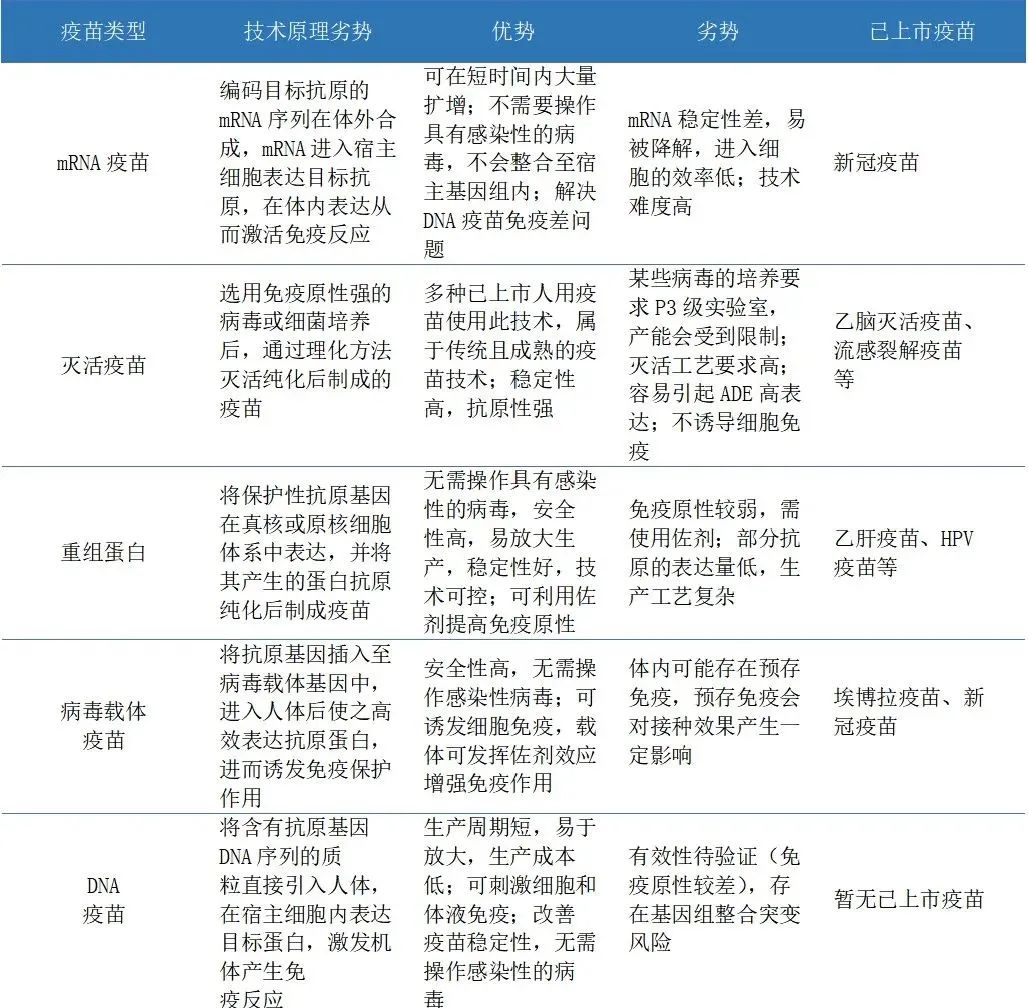
表2:mRNA疫苗与其他路径疫苗比较
更高的开发成功率是mRNA疫苗相对于其他疫苗的优势,未来15年预防性疫苗将在mRNA领域占据主导地位。
预防性疫苗短期内大部分收入仍将来自COVID-19产品,但从中长期看,用于呼吸道合胞病毒和流感等疾病的其他疫苗可能覆盖更广泛的人群,不过价格上涨空间有限。考虑到主要适应症的目标人群渗透率、定价和竞争,估计预防性mRNA疫苗类药物(除COVID-19疫苗以外的产品)的平均全球销售额峰值约为8亿美元。到2035年,经风险调整后的总市场规模为70-100亿美元(不包括COVID-19疫苗)和120-150亿美元(包括COVID-19疫苗)。
考虑到目标人群规模、不同治疗模式的竞争、定价、市场渗透和风险增加等因素,个性化癌症疫苗产品的平均销售峰值约为50亿美元,针对单一疾病产品的销售峰值约为13亿美元。到2035年,整个市场规模(经风险调整)估计将达到70-100亿美元。
治疗性药物可能会是mRNA药物中最大的机会,涉及众多适应症,但mRNA药物是否比其他疗法具有临床优势目前尚不清楚,也有很高的临床风险。长期的机会将取决于诸如递送系统和基因编辑等领域的技术进步。预计治疗性药物将占mRNA产品10%-30%的份额。肿瘤、呼吸系统疾病(主要是囊性纤维化)和罕见病全球管线产品平均销售峰值分别约为11亿美元、18亿美元和5亿美元,并估计2035年整体风险调整后的市场规模为4-50亿美元。
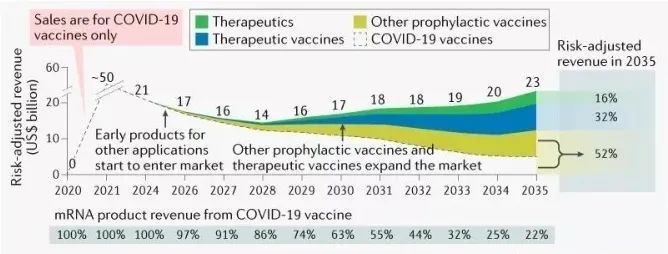
mRNA产品的市场规模短期内取决于COVID-19疫苗的销售,2021年预计将超过500亿美元。在2023-2025年间,由于主流市场对COVID-19疫苗的需求下降,缺乏新产品推出,这一数值将下降,加强针的批准和更广泛的全球使用预计能支撑起200亿美元的销售额。随着其他预防性疫苗和治疗性疫苗产品的推出,mRNA药物市场预计从2028年开始增长,2035年将达到230亿美元。其中,预防性疫苗仍将是基石,2035年的市场份额占比会超过50%。癌症治疗性疫苗占比大约30%,治疗性药物占比不到20%。
mRNA产业链上游为原材料主要包括设备、原材料(DNA质粒、酶、脂质以及分离纯化材料等);中游为药物、疫苗研发生产企业;下游为冷链运输、医院和患者。

图12:mRNA产业链分析
上游包括:DNA质粒模板的制备、mRNA原液的制备、制剂的生产,是整个mRNA产业链中生产成本占比最高的环节,同时也是技术壁垒的关键体现,因此主要对上游中的原材料和生产设备进行分析。
1) 质粒
质粒生产具有先发优势明显,技术积累不易突破的特点。DNA的规模化生产以质粒为载体,核心在于质粒设计、菌株选择、发酵方式、质粒纯化等。DNA的规模化生产类似于抗体生产,依赖于细胞的扩增。
质粒的大规模生产历史不长,各环节多个参数均会影响质粒最终得率,龙头公司技术积累多年形成一定壁垒,包括产量、成本、产物中超螺旋结构比例等,先发优势较为明显。质粒占整个生产成本的9%。
2) mRNA转录与修饰
专利壁垒(修饰核苷酸,帽子类似物CleanCap)高,加上产能难放大(加帽酶),是生产环节中成本占比最大,约56%。
6.1 艾博生物
6.2 斯微生物
6.3 丽凡达/艾美疫苗
6.4 深信生物
6.5 尧唐生物
6.6 嘉晨西海
6.7 瑞吉生物
6.8 蓝鹊生物
7.1 mRNA具备研发生产优势
根据《mRNA技术迎来快速发展期,未来前景广阔》报告显示,以mRNA疫苗为例,其平均研发周期为0.8-1.5年,工艺生产建造周期为2-4年,整体的商业化进程较传统路径快10倍。整体费用是传统路径的1/18。因此,mRNA疫苗在研发、生产周,资金投入方面显著优于其他技术路径疫苗。
mRNA的运用场景不仅限于传染病预防,在肿瘤免疫治疗、蛋白质替代疗法以及再生治疗等领域均有显著优势。国际mRNA巨头在肿瘤治疗领域部署了丰富的研发管线,包括针对黑色素瘤、淋巴瘤等瘤种的产品。
2020新冠疫情,让mRNA技术一度成为疫情防控的焦点,成为结束疫情,让世界回到正常的核心方案。这一现象加速了资本对mRNA的关注,比如2019年成立的艾博生物,至今已完成了6轮融资,融资超11亿美元,根据公开信息其估值已达200亿元人民币,投资机构包括了软银投资、五源资本、高瓴资本等知名机构。同时上市公司也纷纷布局mRNA领域,如沃森生物与艾博生物、蓝鹊生物联合开发mRNA产品。短期内,资本的蜂拥而入,一定程度上透支了行业预期,若后续产品无法落地,验证其商业价值,行业将进行重构。






