以下文章来源于赛柏蓝 ,作者四月的雨
01
为什么90%的药物临床失败?
药物研发是一个漫长、昂贵且充满风险的过程,一招不慎满盘皆输。因为一款新药的研发一般需要10~15年的时间,而且每款新药的平均成本为10~20 亿美元。
虽然任何一家制药公司候选药物进入临床前阶段都经过了严格筛选以及优化,但是在进入临床研究后,90%的候选药物依旧会在I、II、III期临床试验中折戟沉沙。
这也仅是进入临床的药物,如若算上临床前就失败的药物,恐怕失败率将更高。
对2010年至2017年临床试验数据进行分析,90%的药物临床失败主要有四个原因:
(1)缺乏临床疗效,占40%~50%;
(2)难以控制毒性,占30%左右;
(3)药物的不良反应,占10%~15%;
(4)缺乏市场需求,占10%左右。
一般来说,药物研发遵循一个过程,如靶点验证、药物候选分子的高通量筛选、针对活性和药物特性进行严格的药物处方及工艺优化、临床前疗效和毒性测试以及生物标志物指导的患者选择和最佳临床试验设计等。
下图为药物研发基本过程以及每个步骤所花费的时间以及失败的概率。
图1 药物研发过程
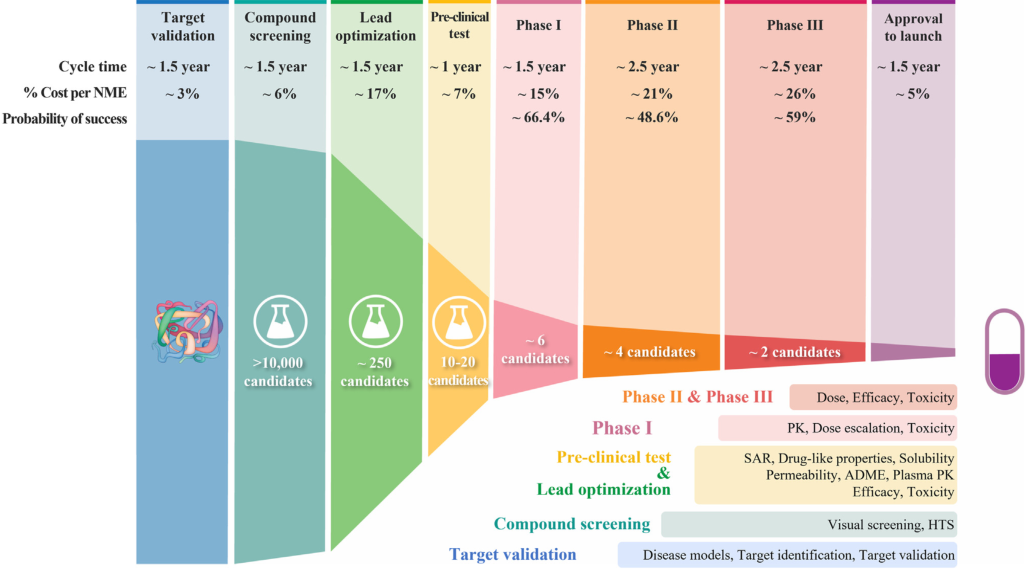
上述药物研发的每一步都经过了严格的优化和验证,以选择最佳的候选药物进行临床研究。尽管做出了这么多的努力,临床药物研发的总体成功率仍然很低。如此高的失败率引发了几个问题:尽管筛选以及优化已经很严格了,为什么还是有90%的临床药物失败了?我们是否忽略了一些什么而导致高失败率?如何提高临床药物研发的成功率?
02
过去的几十年中,药物研发中有哪些关键的策略?
(1)选择最佳的先导化合物以满足临床需求
由于40%~50%的药物研发临床失败是由于缺乏疗效,因此在临床前和临床研究中提高药物疗效一直是我们的首要目标。在药物优化过程中,通过结构活性关系对先导化合物进行广泛的优化,以获得高的靶点亲和力。
其次,选择最佳的先导化合物以最大限度地减少临床毒性也一直是必不可少的一步。药物的毒性可能是由于对靶点的脱靶或靶上抑制造成的。为了降低脱靶毒性,通常针对其他靶标进行药物筛选。
例如,开发任何激酶抑制剂通常需要针对其他数百种激酶进行筛选。另一方面,如果候选药物具有靶上毒性,这是由疾病相关靶点的抑制引起的,则解决方案受到限制,这种情况主要还要依靠剂量来解决。最后,候选药物也可能引起化学诱导的毒性,而没有明确的已知靶点。
第三,我们应选择的化合物最好具有一定的类药性。上世纪90年代,有30~40%的药物研发失败是由于所选的先导化合物类药性不佳。而目前失败率已经降至10%左右,正是得益于类药性的选择,包括溶解度、渗透性、蛋白质结合、代谢稳定性和体内药代动力学如生物利用度等。
(2)优化药物研发战略
战略方向的错误也是导致临床失败的一部分因素,占药物研发失败的10%左右。制药公司应制定细致的研发计划,详细制定研发的各个阶段,以推动新化合物通过每个研发阶段。由经验丰富的专家组成多学科项目团队,在各种商业模式和分析工具的帮助下共同制定战略规划。人工智能使制药公司能够以更有效和更具成本效益的方式预测患者的需求和市场趋势。
03
药物研发中哪些被忽略的因素导致了高临床失败率?
(1)靶点验证
靶点验证主要有两方面内容。第一就是确认该靶标确实是导致人类疾病的原因。虽然在体外细胞系、动物疾病模型和人类疾病模型中使用各种遗传或基因组方法对这类靶标验证进行了广泛的研究,但分子靶标的生物学差异仍然存在于体外和体内之间,或动物和人类疾病之间。在现实中,一个分子靶点在成功研制出药物之前不会被完全验证,这给药物的开发带来了挑战。
第二,确定分子靶标是否为药物分子的预期靶标。通常通过SAR研究结合分子靶标的特异性、亲和力来确定。但是药物靶点的验证具有挑战性,因为药物的药理作用(药效以及毒性)可能是由于抑制了与预期靶点不同的未知分子靶点造成的。
(2)过分强调某一方面,而忽略其他方面
在药物优化过程中,对化合物进行严格优化的主要有两个方面:
(1)通过SAR对先导化合物抑制分子靶标特异性进行严格优化,即在低nmol/L甚至pmol/L范围内,要求较低的Ki或IC50,以获得更好的疗效,减少脱靶效应;
(2)先导化合物的类药物性质也被广泛优化,使用一定的临界值作为药物溶解度、渗透性、稳定性、蛋白结合和血浆PK参数的可接受标准。但药物开发的成功率仍然保持在10~15%。持续的高失败率导致了一个问题,即药物优化的某些方面是否被忽略了?
在临床药物开发中,需要在临床剂量、疗效和毒性之间实现微妙的平衡,以优化患者的受益/风险比。理想的候选药物应具有高效力和特异性,以抑制其分子靶点而不产生脱靶效应,理想情况下是低剂量获得足够的疗效,并在最佳剂量下减少在健康组织中的药物暴露,以避免毒性。目前的药物优化过程可能过于强调利用SAR研究的效价以及特异性,而忽视了疾病靶向组织与健康组织中药物的平衡,从而误导了药物候选的选择,使临床剂量、疗效、毒性失衡,导致临床失败率较高。
04
平衡临床剂量、疗效与毒性,提高临床药物开发成功率?
临床药物开发的成功与否取决于最佳候选药物的选择,以及临床剂量、疗效与毒性之间的微妙平衡,以及真正的靶标验证。
我们可以设计一个特异性及效力、疾病靶向组织中的暴露和选择性系统(STAR)来改进药物优化过程。STAR系统根据三个方面将候选药物分为4类(I-IV类)。四种不同类别的候选药物(I-IV类)需要不同的策略来选择先导药物,优化临床剂量,平衡临床疗效与毒性。
图2 利用STAR进行药物选择
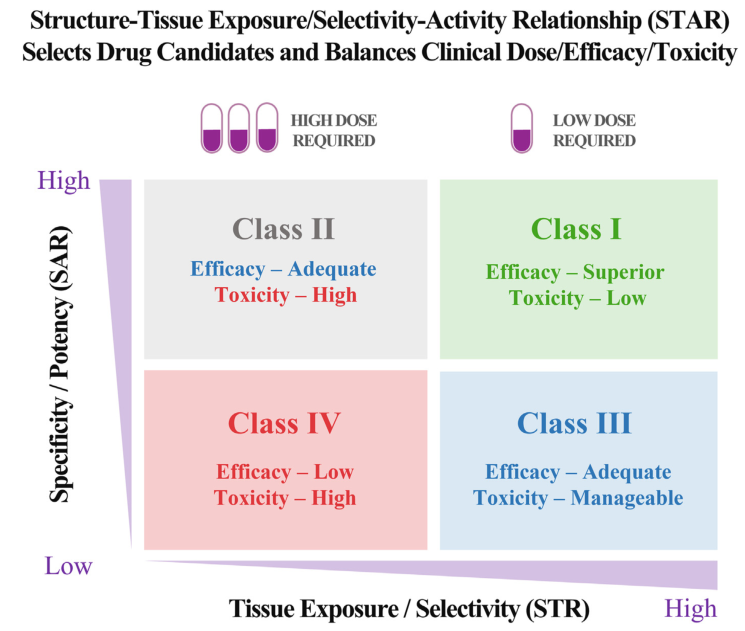
I类候选药物对分子靶标具有高特异性及效力,并且在疾病靶向组织中的高暴露和选择性。I类候选药物需要低剂量就能达到足够的疗效,健康器官中的毒性较低,这得益于疾病组织的高选择性和正常器官中的低组织暴露。I类候选药物也是最理想的。例如,以下成功获批的药物很可能是I类药物,如抗病毒药物索非布韦、胆固醇治疗药物阿托伐他汀、勃起功能障碍治疗药物西地那非。
II 类候选药物对分子靶标具有高特异性及效力,并且在疾病靶向组织中的低暴露和选择性。为了在疾病靶向组织中获得足够的疗效,II 类候选药物通常需要高剂量,因此毒性可能变得难以控制。此类药物需要进行优化,以提高特异性。几种药物可能是II类药物,例如抗癌药ibrutinib、spebrutinib和fedritinib。
III类候选药物对分子靶标具有低特异性及效力,并且在疾病靶向组织中的高暴露和选择性。III类候选药物需要低到中等剂量才能达到足够的疗效,由于剂量偏低,毒性是可控的。但是这类药物由于低靶标活性,它们通常在药物优化阶段就被淘汰了。市场上属于III类药物的很少,因为许多III类候选药物可能已在早期药物发现过程中终止。抗癌药沙利度胺可能属于III类药物。
IV类候选药物对分子靶标具有低特异性及效力,并且在疾病靶向组织中的低暴露和选择性。此类药物可以说是最不受欢迎的,大多数IV类候选药物在临床开发中都是失败的,成功的例子非常有限。
临床失败的药物比比皆是,原因主要为缺乏临床疗效、毒性难以控制以及类药性差。我们可以利用STAR系统,通过人工智能建模以及体外筛选, STAR的应用将提高四种不同类别候选药物的药物优化和临床研究效率,从而提高临床药物开发的成功率。
参考文献
[1]Why 90% of clinical drug development fails and how to improve it?
[2]孙学军, 邓泮. 药物临床试验失败,企业损失数亿美元[J]. 2012(33).






