照片为我国为边境少数民族孩子种痘,图片来源于网络。
●1937年瑞典物理学家Arne Wilhelm Kaurin Tiselius通过电泳技术证明了抗体也是一种蛋白质,并将其称为γ球蛋白。
●1953年英国生物化学家Frederick Sanger成功解析了同样身为蛋白质的胰岛素的化学结构,从而为科学家们解析抗体结构指明了方向。
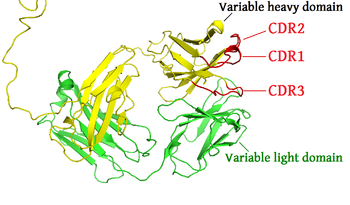
●1963年,Edelman与RodneyRobert Porter(Sanger的第一个博士研究生)结合两人多年的研究结果,提出了比较成熟的“Y”型对称结构的抗体分子模型。
●1969年,Edelman和Porter完成了一项在当时了不起的成就,他们成功对抗体1300多个氨基酸序列进行了测定,是当时测定氨基酸序列的最大的蛋白质分子。
IgG是血清中一种主要的Ig,含量占总Ig的65—75%左右。广泛分布于组织液中,血管内、外间隙中分布量大体相当。是机体抗感染的一种重要物质。 IgM是成熟胎儿合成的第一类Ig,也是在感染或免疫后最早产生的Ig,5类Ig中IgM最强,故其细胞毒活性和细胞溶解活性也最强。天然的血型抗体是IgM,有些自身抗体如抗磷脂抗体、RF等也属于IgM。胎儿脐血中IgM抗体升高,是胎儿遭受感染的标志。 IgA在血清和组织液中的含量相对较少,血清型IgA含量占总Ig的15—25%,但在外分泌液如初乳、唾液、眼泪、肠道分泌液和支气管分泌液中含量较高。由于IgA主要存在于外分泌液中,故在第一线抗感染防御中起重要作用。 IgE为单体结构,是正常人血清中含量最少的Ig。IgE在血清和组织液中含量极微,其主要生物学功能是与组织肥大细胞、嗜碱粒细胞表面的特异受体结合。IgE不能激活补体。IgE含量在正常人群波动较大,在特异性过敏反应和寄生虫早期感染患者血清中可升高。当变态反应原与结合在受体上的IgE反应时,可引起肥大细胞、嗜碱粒细胞脱颗粒,释放出组织胺、5—羟色胺等生物活性物质。 IgD在正常人血清中IgD浓度很低,几乎检测不到。IgD主要存在于人B淋巴细胞表面作为抗原的细胞受体,在血清中IgD含量极微且与膜结合的IgD有不同结构。B细胞上IgD的可变区与该细胞将分泌的IgG、IgA、IgM的可变区相同,当抗原与IgD受体结合时,刺激B细胞繁殖、分化、并分泌对抗原特异的其他类抗体