以下文章来源于抗体密码 ,作者抗体密码-大脸猫
双特异抗体作为能够同时结合两种不同抗原的抗体,其在作用机制方面有更多的发挥空间。双特异抗体已经在血液瘤中取得的成功,目前已经有两款双抗获批上市,包括靶向CD19/CD3的双抗blinatumomab和靶向CD20/CD3的双抗Mosunetuzumab,而且还有众多靶向血液瘤的双抗在临床中取得了不俗的疗效。但是在实体瘤的治疗中,目前仅有强生的双特异抗体amivantamab(EGFR/cMET)获批上市,并且众多靶向激活T细胞的双抗在实体瘤中因为毒性等问题无法达到预期效果。
ADC药物,作为一种靶向递送毒物的药物,在实体瘤的治疗中取得了较大成功。作用机制不同于通过机体免疫系统杀伤肿瘤的双抗药物,ADC主要是通过其载荷对肿瘤细胞进行抑制杀伤,但是目前的ADC药物同样也是因为毒性问题无法达到最佳的治疗窗口。那么双特异抗体联合ADC会是怎样的效果呢,能否做到扬长避短?从目前的临床前数据来看,部分双抗ADC不仅比裸抗具有更好的疗效,而且具有良好的安全性,但是其最终效果还需要在临床中验证。本篇文章我们来盘点并介绍一下目前已知的一些在临床中,或者临床前的双特异抗体ADC的临床前数据。
ZW-49
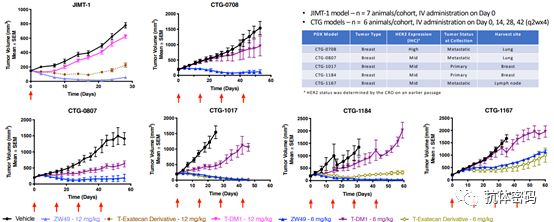
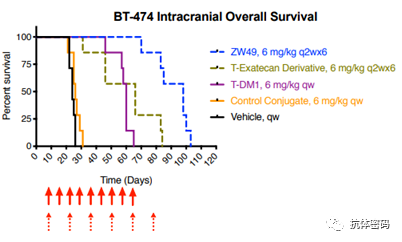
ZW-49是由Zymeworks开发的双特异性抗体ADC药物,可同时特异性结合HER2受体的两个非重叠表位(ECD4/trastuzumab和ECD2/pertuzumab),该双特异抗体ADC是在ZW25的基础上通过蛋白酶切割链接子偶联Auristatin毒素A。在临床前的NHP动物模型中,该双抗ADC的最高耐受剂量到达18mg/kg。

BL-B01D1
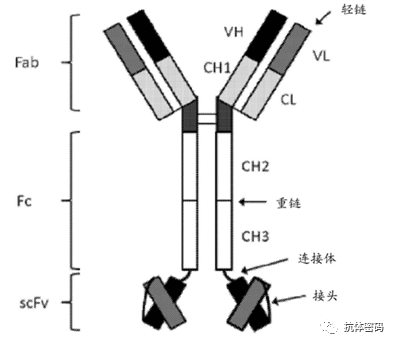
BL-B01D1是由百利药业开发的靶向EGFR/Her3的双特异抗体ADC,除了双抗ADC,目前百利药业也布局了EGFR/Her3的双特异抗体,从其发表的专利来看,EGFR/Her3双抗的结构可能如下图所示,为完整抗体上融合scFv的2+2对称型结构(以企业披露为准)。
作用机制方面,BL-B01D1不仅可以同时阻断EGFR、HER3与配体的相关结合,而且其与EGFR、HER3结合后可以通过细胞内吞进入细胞内部,由水解酶酶切释放小分子毒素ED04,阻止肿瘤细胞的DNA复制和RNA合成,并破坏DNA结构,从而进一步杀伤肿瘤细胞,目前该药物已经在国内进入临床。
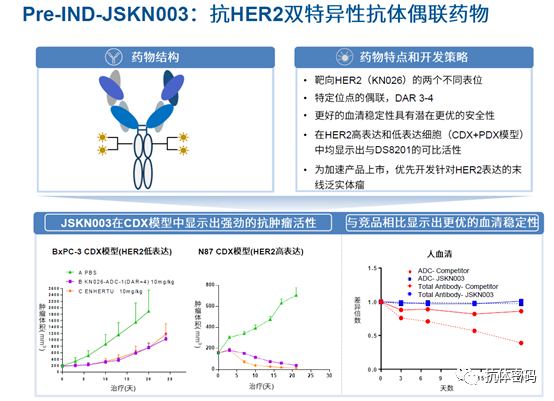
JSKN003
REGN5093-M114
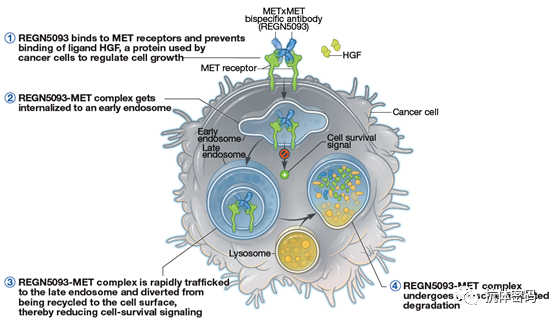
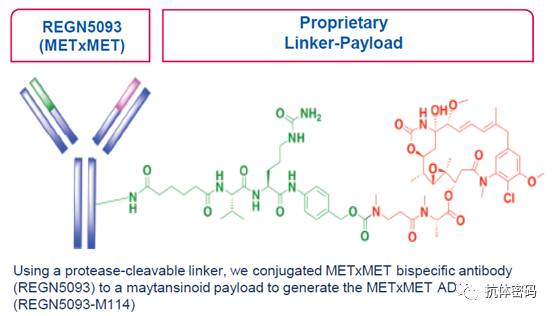
REGN5093- M114是是由Regenron开发的靶向MET两个不同表位的双抗ADC,该抗体为1+1非对称型双特异抗体,通过M114 linker将抗体与毒素M24(美登素衍生物)连接,DAR值为3.2左右。其可以同时结合两个MET的不同的表位,并可以有效的阻断HGF与MET的结合,从而可以防止相关通路的激活;另外,抗体结合肿瘤细胞表面的MET后,抗体和MET形成的2+2型复合物可以被内化,进入肿瘤细胞并在溶酶体中被降解,从而可以减少MET通过再循环表达在细胞表面。除此之外,REGN5093- M114中可以被酶切的linker在溶酶体中被酶切后释放M24毒素并通过作用于微管蛋白来抑制肿瘤生长。
与其它抗体不同,REGN5093- M114裸抗本身同样具有一定的抑制肿瘤的效果,并且在临床前的多种模型中展现了良好的药效,目前再生元已经将裸抗REGN5093和ADC双抗REGN5093- M114 两种药物都推向了临床。
M1231
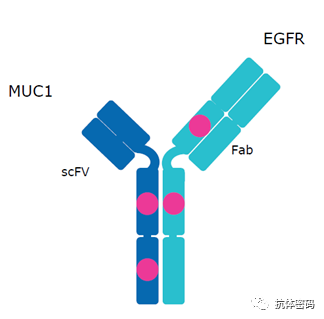
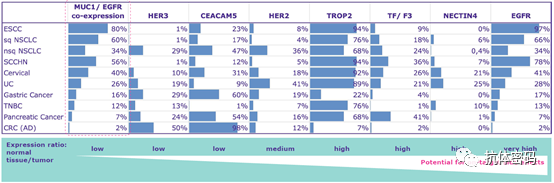
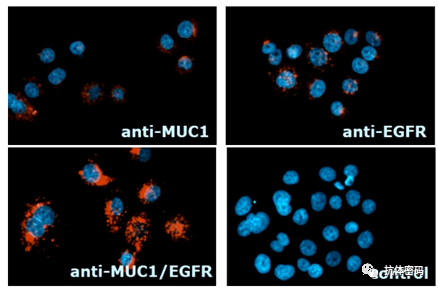
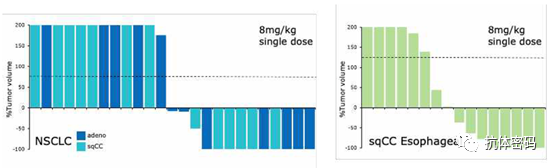
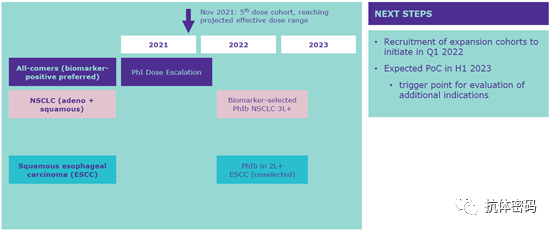
默克之所以选择MUCI/EGFR作为靶标,是因为相关研究表明,MUCI/EGFR共表达在多种肿瘤细胞中,如ESCC,NSCLC,SCCHN等,而且其共表达在正常组织中非常低,因此理论上可以降低On-target毒性,提高用药窗口。另外,其研究表明抗体同时结合肿瘤表面的两种抗原,使得抗体快速内吞,并释放响应的毒素抑制肿瘤细胞的生长。
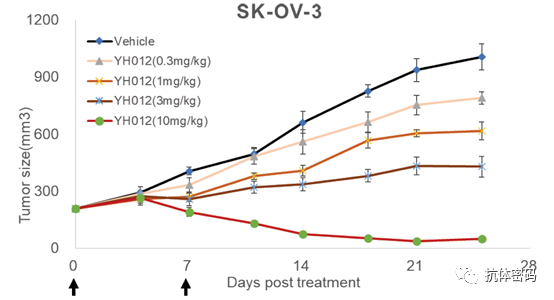
百奥赛图双抗ADC YH012
百奥赛图的双抗ADC是在其RenLiteTM双特异抗体平台上构建的, RenLiteTM利用共同轻链的方法防止双特异抗体轻链的错配,同时采用Knob-In-Hole防止抗体重链错配,该平台可以实现高纯度双特异抗体的生产。在此基础上,其利用链间半胱氨酸进行偶联,linker为可裂解的二肽VC(valine-citrulline),毒素为MMAE。
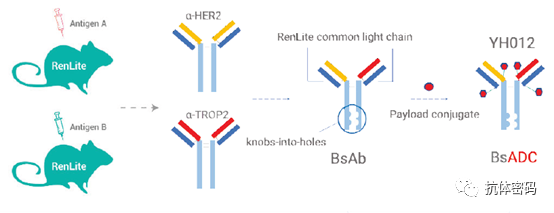
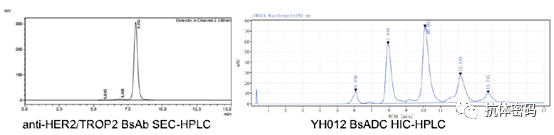
图片来源:百奥赛图官网
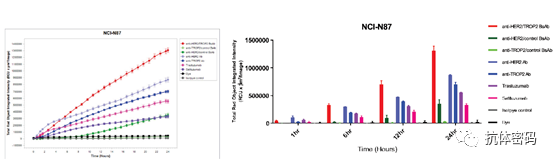
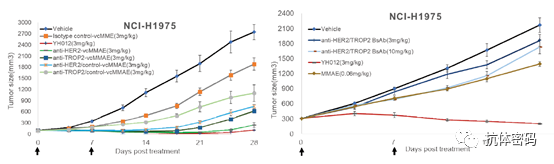
双特异抗体比较复杂,其药效与抗体的靶点组合,抗体的结构,两个抗体的亲和力等相关;ADC也比较复杂,其药效与抗体,linker和毒素等相关;因此双抗ADC会更加复杂,其设计需要对双抗的作用机制,ADC的原理等都具有深刻的理解。目前双抗ADC才刚刚起步,多数处于临床前期,从现在的临床前部分数据来看,双抗ADC具有比裸抗更好的疗效,但是安全性,有效性还是需要到临床中验证。






